作為長期深耕該領域的CRO,向外,我們期待中國企業在全球競爭中嶄露頭角,打破復雜制劑進口壟斷;向內,我們希望與行業所有的參與者一起,找到應對競爭的航向與路徑。
做行業的“記錄者”與“同行者”,聚焦經皮領域藥物研發及審評動態的持續追蹤和分享,以下是「晶易TDDS觀察」首期文章。
2025年1-2月核心數據速遞
審評數據:仿制加速,創新升溫
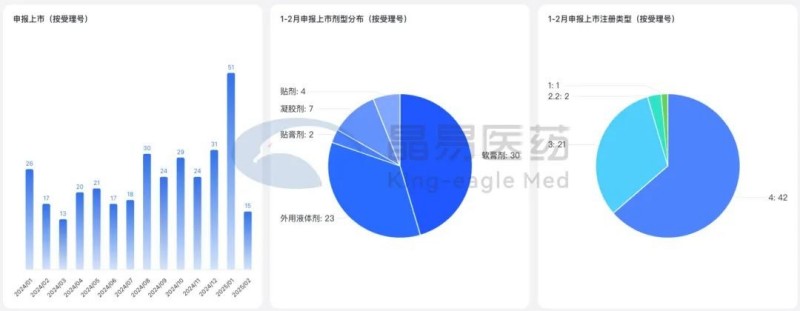
CDE受理經皮給藥上市申請66項(同比+54.8%),1月環比創新高(51項),軟膏劑占45%,化藥貼膏劑(氟比洛芬、洛索洛芬鈉等)再增4家,企業扎堆布局,江蘇恒瑞的首款國產jak1抑制劑艾瑪昔替尼軟膏申請上市。
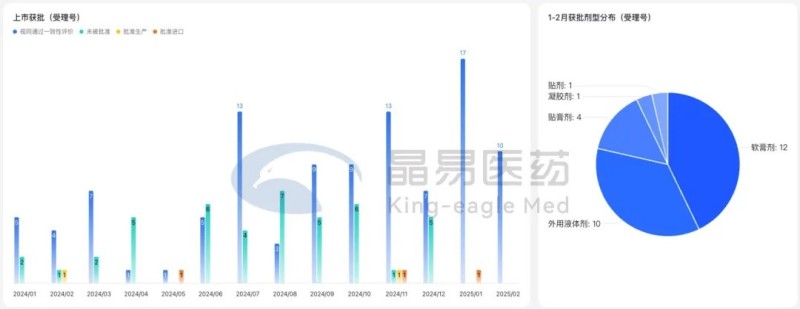
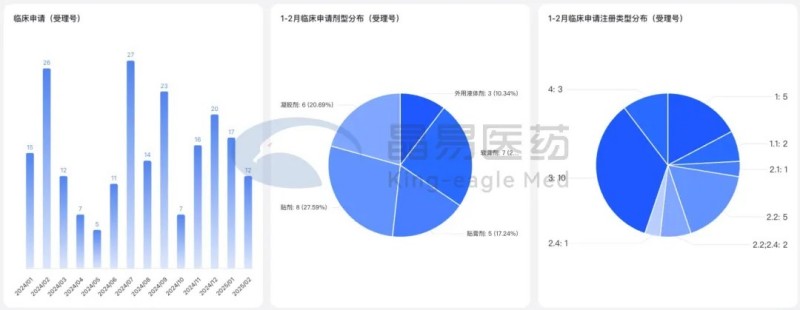
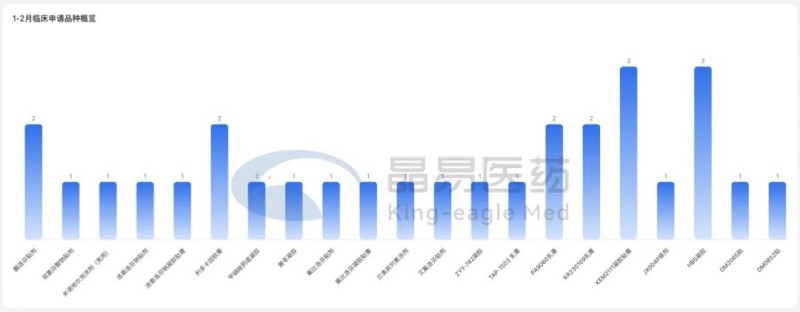
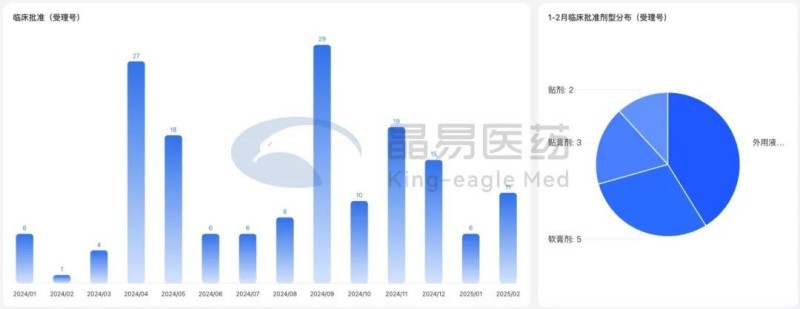
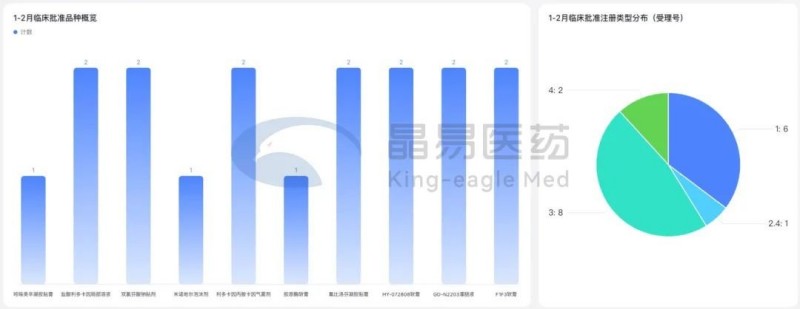
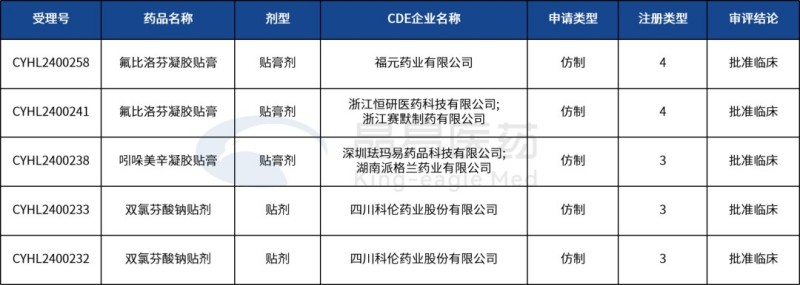
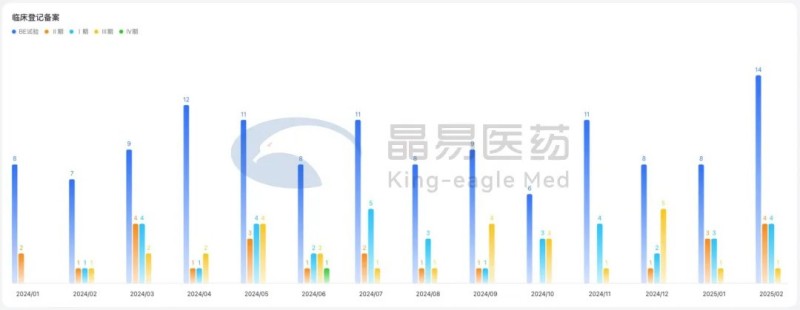
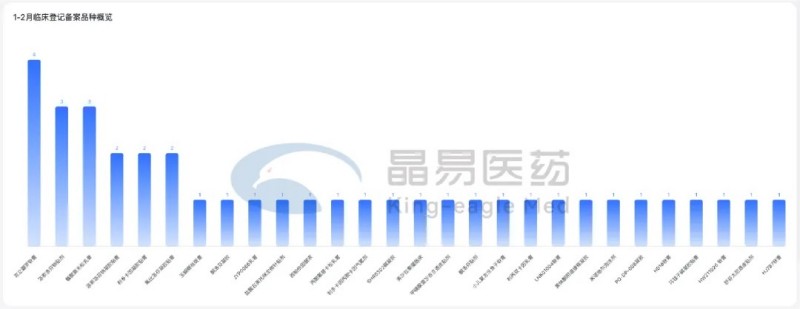
CDE批準17項臨床試驗(同比+143%),貼膏/貼劑占半壁江山;4個1類/1.1類新藥臨床申請獲受理,3個1類新藥臨床申請獲批準;6個改良型新藥臨床申請獲受理。
過評數據:頭部品種“廝殺”加劇
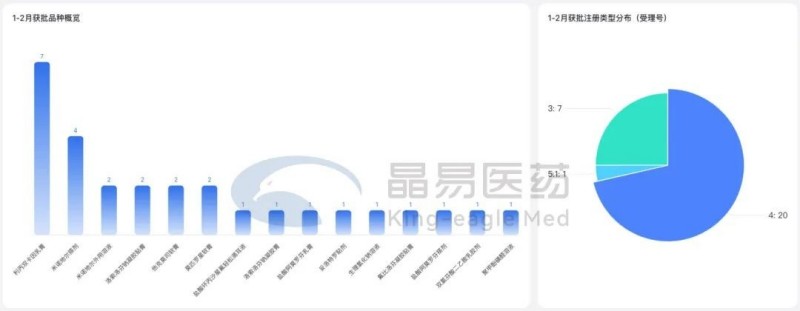
一致性評價破紀錄:27個上市批準,1月過評數量環比創單月新高(17個),共涉及13個品種,其中利丙雙卡因乳膏通過7項(按受理號)、米諾地爾搽劑/外用溶液通過6項(按受理號)。
核心品種預警:氟比洛芬凝膠貼膏(8家審評中,6家已完成/正在開展BE)、洛索洛芬鈉凝膠貼膏(13家審評中,5家已完成/正在開展BE)等4個品種申報企業超10家,最快2025年下半年納入集采,百億市場洗牌在即。
一、上市審評動態
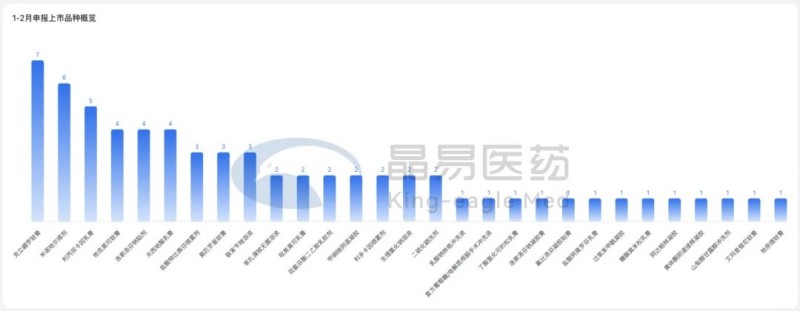
從1-2月上市審評數據看重點品種情況
克立硼羅軟膏,新增7個上市申請受理號,涉及6家企業,除2024年10月過評的南京萬融健誠醫藥、齊魯制藥外,仍有27家上市申請審評中。
米諾地爾搽劑/溶液,外用制劑最卷品種之一,1月-2月新增福元藥業、四川科倫、浙江鼎泰、江蘇晨牌邦德過評。同時新增受理號6個,涉及3家企業。
利丙雙卡因乳膏,受醫美市場整頓“麻膏”產品的影響,該品種從2024年12月開始進入批文激增,其中1-2月新增7家過評(廣州朗圣、蘇州二葉、德全藥品、四川科倫、江西施美、浙江賽默、渼顏空間),同時新增受理號5個,涉及4家企業。
氟比洛芬/洛索洛芬鈉凝膠貼膏,1-2月最高熱度品種,繼樂明藥業、武漢法瑪星、北京泰德、南京海納、湖南金圃等企業過評后,1-2月新增上市申報福元藥業(氟比洛芬凝膠貼)、浙江昂利康(洛索洛芬鈉凝膠貼)。百億貼膏市場加速洗牌,氟比洛芬、洛索洛芬鈉等品種申報企業超15家,集采臨近。
黃體酮陰道緩釋凝膠,至今無國產上市的高難度品種,此前報產均因復雜制劑技術壁壘遭駁回。仙琚制藥自2022年8月首輪申報后,歷經CDE多輪技術審評,近期補充材料再戰審批,若仙琚制藥成功拿下首仿,將填補國產空白并直接挑戰原研雪諾同(Merck Serono)在華的壟斷地位。
地奈德軟膏,1-2月報產的3類仿制藥中唯一一款軟膏劑,新增申報企業湖南明瑞制藥,首家報產的杭州領業目前處于發補審評中,兩家企業均由長沙晶易醫藥提供研發服務。
二、臨床審批動態
出品:湖南省貼劑類經皮遞藥系統工程技術研究中心
注:本文數據均來源于摩熵醫藥。統計數據僅供參考,如有疏漏,歡迎指正!轉載請聯系15616185772,并注明來源和作者。


